Magali M. Silva
Atualizado - Março 2022
Introdução
O diagnóstico de endocardite pode ser difícil, devido sua natureza multifatorial. Cerca de 90% dos pacientes apresentam febre, e 85% apresentam um novo sopro, ou alteração no sopro pré-existente. Quadros atípicos são comuns em idosos e pacientes imunocomprometidos (muitos podem não apresentar febre, por exemplo).
Assim este protocolo tem como finalidade uniformizar o atendimento ao paciente suspeito e definir condutas terapêuticas.
Classificação
E.I. segundo a localização e presença ou ausência de material intracardíaco:
E.I. de valva nativa esquerda
E.I. de valva protética esquerda
E.I. direita
E.I. relacionada a dispositivo (desfibrilador, marca-passo definitivo)
E.I. segundo o modo de aquisição
E.I. relacionada à assistência à saúde:
Nosocomial: doença com início dos sinais e sintomas durante a internação do paciente, considerando-se que o mesmo foi admitido fora do período de incubação da doença; que pode variar de acordo com a apresentação clínica e agente infeccioso. Considerar, nas EI nosocomiais, também agentes etiológicos menos frequentes, como Candida e bacilos gram-negativos não-HACEK
Não-nosocomial: sinais e sintomas de EI iniciam fora do hospital, ou na internação, caso o paciente tenha sido admitido dentro do período de incubação da doença, em paciente com algum dos critérios:
Homecare, hemodiálise ou quimioterapia EV <30 dias antes do início dos sinais/sintomas
Hospitalização <90 dias antes do início dos sinais/sintomas
Paciente residente em asilos/instituições de cuidados crônicos
E.I. adquirida na comunidade:
Sinais/sintomas da doença se iniciam no ambiente comunitário, ou na internação, caso o paciente tenha sido admitido dentro do período de incubação da doença, em pacientes que não preencham os critérios listados acima;
E.I. associada ao abuso de drogas ilícitas endovenosas;
E.I. Segundo a recorrência
Relapso: Repetição do episódio de EI, causada pelo mesmo microorganismo, <6 meses depois do episódio inicial.
Reinfecção: Infecção por um microorganismo diferente, ou episódio repetido pelo mesmo microorganismo, >6 meses após o episódio inicial.
E.I. Segundo critérios microbiológicos
E.I. com hemoculturas positivas (agentes mais comuns):
EI por estreptococos e enterococos: estreptococos do grupo viridans fazem parte da flora oral, e compreendem espécies como S. Sanguis, S. mitis, S. salivarius, S. mutans, e Gemella morbillorum. Esses microorganismos são sempre sensíveis à Penicilina G. O grupo ‘S. anginosus’ (S. anginosus, S. intermedius e S. constellatus) se distingue pela tendência a formar abscessos e causar infecção hematogênica disseminada; sempre requerem antibioticoterapia mais prolongada. Estreptococos do grupo D formam o complexo S. gallolyticus/S. equinus, e incluem espécies comensais do trato intestinal humano. São sensíveis à Penicilina como os espreptococos orais. Entre os enterococos, E. faecalis, E. faecium e, menos frequentemente, E. durans, são as três espécies causadoras de EI.
EI estafilocócica: infecções em valvas nativas costumam ser provocadas pelo S. aureus, geralmente sensível à oxacilina. Já as infecções estafilocócicas em valvas protéticas também costumam estar associadas a estafilococos coagulase-negativo, que são, em sua maioria, naturalmente resistentes à oxacilina. Entretando, o S. lugdinensis é um coagulase-negativo que costuma estar associado à EI de valva nativa, com curso clínico frequentemente agressivo (comportamento semelhante ao S. aureus).
EI com hemoculturas negativas devido à antibioticoterapia prévia: os microorganismos mais comumente envolvidos são estreptococos orais e estafilococos coagulase-negativos.
EI frequentemente associada a hemoculturas negativas: geralmente causadas por microorganismos fastidiosos, como alguns estreptococos, bacilos gram negativos do grupo HACEK (Haemophilus, Actinobacillus, Cardiobacterium, Eikenella e Kingella), Brucella e fungos.
EI constantemente associada a hemoculturas negativas: causada por bactérias intracelulares, como Coxiella burnetti, Bartonela, Chlamydia. Correspondem a cerca de 5% de todas as EI. O diagnóstico demanda recursos como sorologias, culturas de células e amplificação genética.
Critérios de Suspeição e Diagnóstico

*manchas de Roth: manchas retinianas hemorrágicas
*manchas de Splinter: linhas hemorrágicas sub-ungueais
*lesões de Janeway: lesões eritematosas periféricas, indolores (vasculite)
* nódulos de Osler: nódulos periféricos dolorosos, que aparecem principalmente em polpas digitais
Critérios de Duke Modificados
Os critérios modificados de Duke auxiliam no diagnóstico, pois possuem sensibilidade e especificidade elevados, mas não substituem o julgamento clínico. É uma ferramenta que deve ser aplicada quando há suspeição clínica de EI, segundo descrito acima. É um método menos sensível para avaliar casos de EI em próteses e em presença de dispositivos intracardíacos, além de casos em pacientes institucionalizados.
Endocardite Infecciosa Definida
Critério patológico:
Microorganismos demonstrados em cultura ou anátomo-patológico de uma vegetação, material embolizado, ou abscesso, ou confirmação histológica demonstrando EI ativa
Critério clínico:
2 critérios maiores ou
1 critério maior e 3 menores ou
5 critérios menores
Endocardite Infecciosa provável
1 critério maior e 1 critério menor
3 critérios menores
Endocardite Infecciosa Afastada
Diagnóstico alternativo confirmado que explique as manifestações clínicas suspeitas de EI
Resolução do quadro com ≤4 dias de terapia adequada
Ausência de evidência patológica de EI em espécimes cirúrgicos ou de necropsia com ≤4 dias de terapia
Não-preeenchimento dos critérios definidos nos quadros acima

Ecocardiograma em EI (Recomendações)
Diagnóstico
Ecocardiograma Transtorácico (ETT) é recomendado com exame inicial na suspeita de EI (IB)
Ecocardiograma Transeofágico (ETE) é recomendado em pacientes com elevada suspeição clínica e ETT normal (IB)
Repetir ETT/ETE é recomendado em 5-7 dias caso inicialmente normal, mas mantida suspeição de EI (IB)
Mesmo em caso de ETT positivo, considerar realizar ETE, que é mais sensível para identificar abscessos e mensurar vegetações (IIaC)
ETE não é indicado em pacientes com ETT negativo e baixa suspeição de EI (IIIC)
Seguimento durante o tratamento
Repetir ETT/ETE é recomendado assim que houver suspeita de nova complicação (novo sopro, embolia, febre persistente, bloqueio, congestão, abscesso) (IB);
Repetir ETT/ETE deve ser considerado durante o tratamento para avaliar complicações silenciosas e redução do tamanho da vegetação (IIaB).
Ecocardiograma intra-operatório
É recomendado em todos os casos de EI que requeiram intervenção cirúrgica (IC).
Seguimento após o fim do tratamento
ETT é recomendado apos o término da antibioticoterapia para avaliação morfológica e funcional do coração e válvulas (IC).
Tratamento
A duração do tratamento da EI deve ser contado a partir da negativação das hemoculturas. Por isso, devem ser colhidos dois pares de amostras de hemoculturas a cada 48h, após início da terapia antimicrobiana.
Caso o paciente seja submetido a cirurgia de troca valvar, deve ser enviado o material retirado para cultura; caso a cultura seja positiva, o tempo de tratamento deve ser reiniciado (pelo menos mais 4 semanas). Caso haja presença de abscesso Peri-valvar, o tempo também deve ser reiniciado, independente de resultados de culturas.

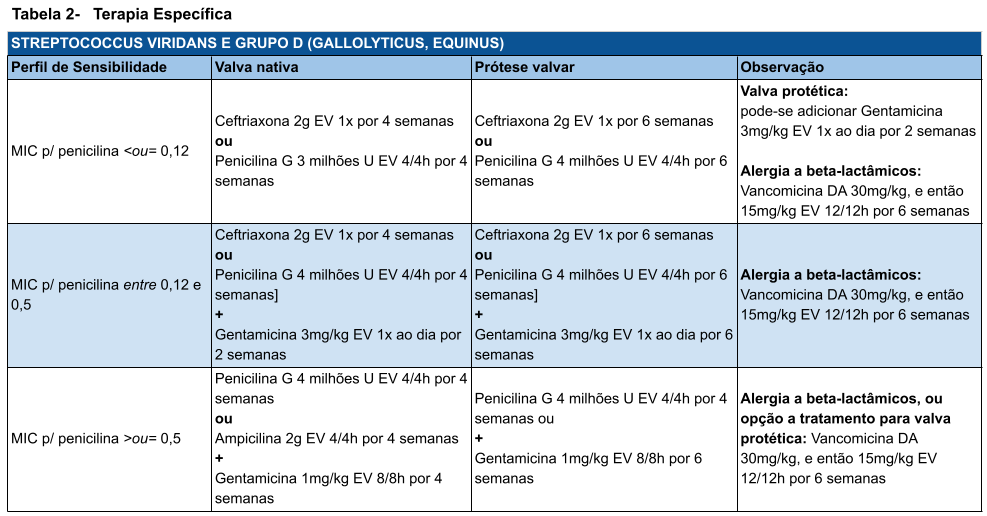



Tabela 3 – Terapia específica para microrganismos menos comuns

Observações
Indicação de intervenção cirúrgica precoce (ou seja, durante o tratamento antimicrobiano):
EI de prótese e dispositivos intracardíacos (retirada dos fios e gerador);
Disfunção valvar resultando em insuficiência cardíaca;
EI esquerda por S. aureus, fungos, gram-negativos não-HACEK e microorganismos multirresistentes;
EI complicada por bloqueio, abscesso anular ou aórtico, lesões infiltrativas;
Pacientes com bacteremia persistente, após 5-7 dias de terapia antimicrobiana efetiva;
Deve ser considerada com episódios embólicos recorrentes e vegetação persistente a despeito da terapia antimicrobiana adequada;
Deve ser considerada em EI de valva nativa com vegetação >10mm (EI esquerda) ou >20mm (EI direita)
Relapso do quadro de endocardite.
Fluxogramas de Tomada de Decisão.
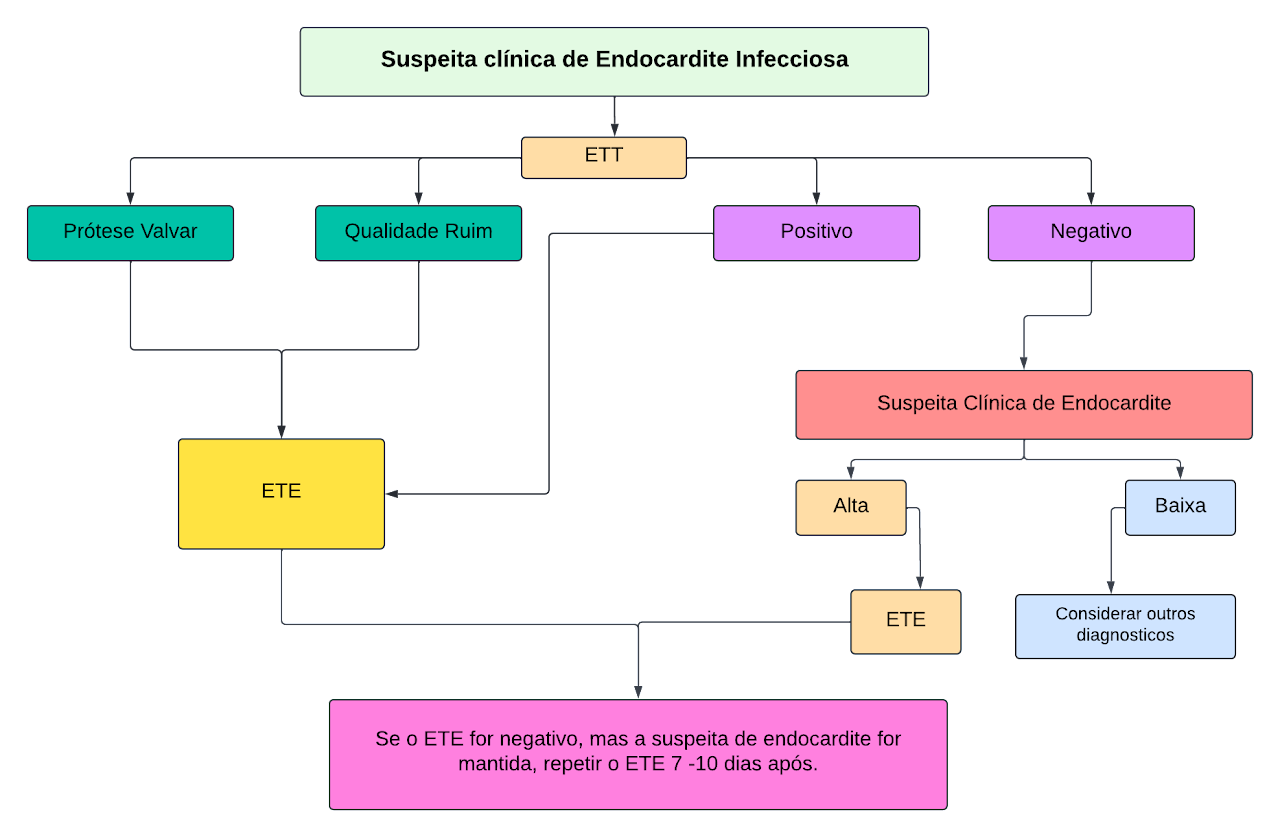
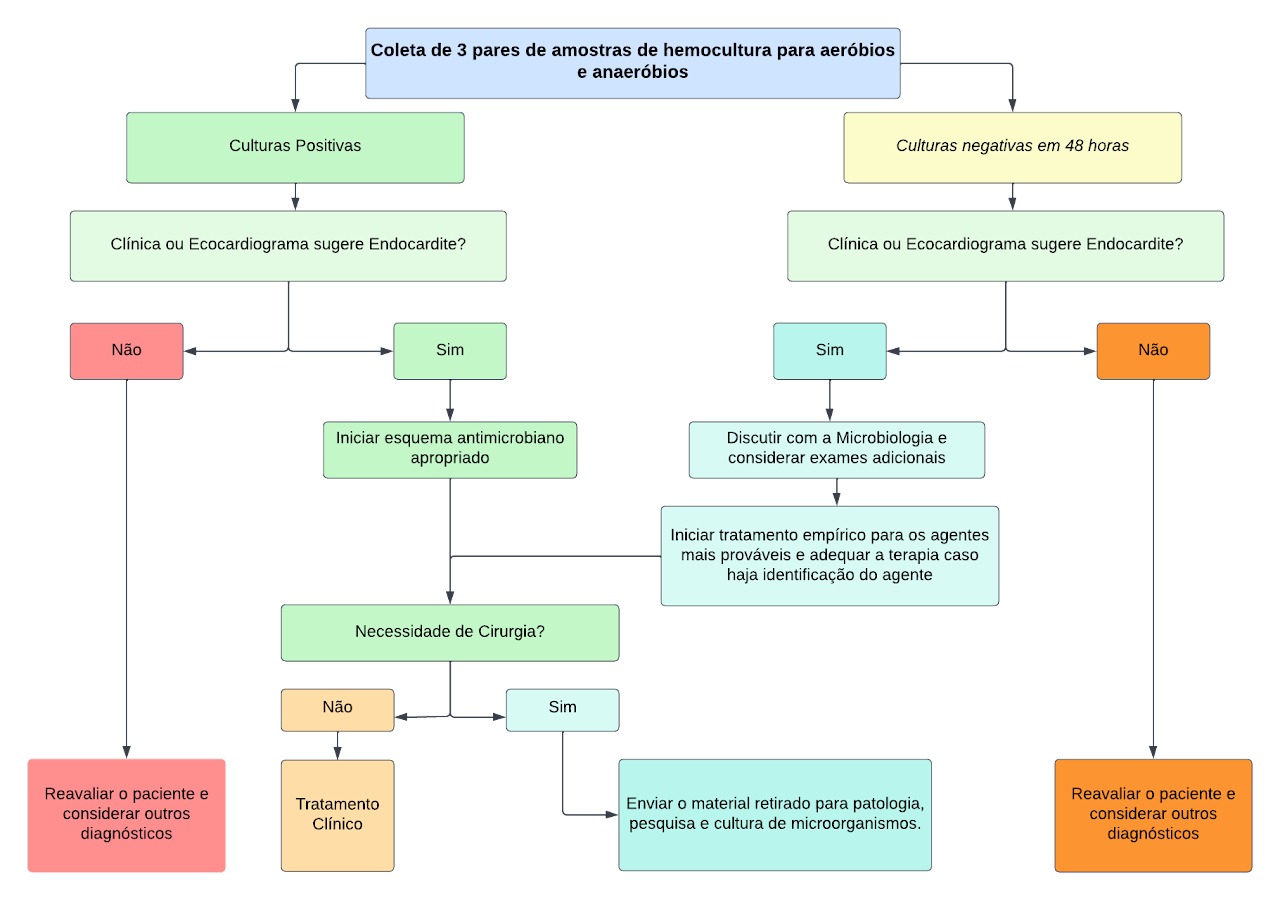
Referências
- ESC Guidelines for the management of Infective Endocarditis (2015)
- Infective Endocarditis in Adults: Diagnosis, Antimicrobial Therapy and management of Complications, AHA/ACC (2016);
- The Sanford Guide to Antimicrobial Therapy (2022);
- Mandell, Douglas, and Bennett’s Principles and Practice of Infectious Diseases, 8th Edition
